Les glucuronoconjugaisons : application dans le cadre du métabolisme des médicaments et des composés toxiques
Graveron élise , Lussiez coralie, Marel juliette, Troitzky karine
I. Introduction
1. Définition
Les Biotransformations des xénobiotiques (xb) ont comme « rôle la protection » de l’organisme. Elles interviennent dans la transformation des xénobiotiques en composés hydrosolubles, éliminables et dans neutralisation de leurs groupements réactifs.
2. Réaction de phase I et II
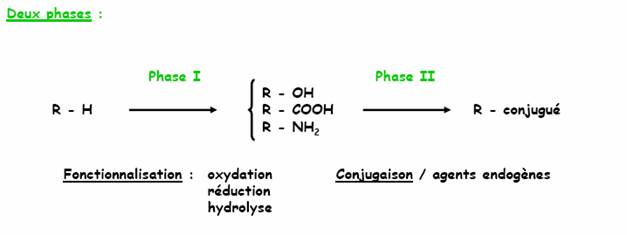

II. Présentation générale
1. Définition :
- Glucuronoconjugaison : réaction de conjugaison de phase II
agents de conjugaison = hydrophiles endogènes
quantitativement la plus importante
La glucuronoconjugaison est la réaction de formation d’une liaison osidique entre l’acide glucuronique et une molécule endogène ou exogène préalablement à son élimination par voie
biliaire ou urinaire.
Ces réaction sont principalement hépatiques et sont catalysées par des UDP-glucuronosyltransférases. Elles constituent une voie de détoxication de l’organisme.
2. Agents de conjugaison
Acide glucuronique activé en acide UDP-α-D-glucuronique dans le cytosol des hépatocytes à partir du glucose 1-phosphate. Très hydrosoluble, permet l’hydrosolubilisation des molécules apolaires, préalablement à leur élimination. Une fois conjuguées, ces molécules perdent leur éventuelle toxicité et le conjugué [molécule apolaire – glucuronate], hydrosoluble, peut être éliminé de l’organisme.
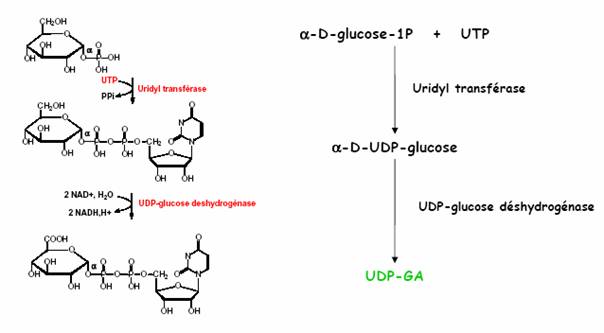
3. Substrats
Les substrats sont endogènes comme les hormones sexuelles (stéroides) ou les acide biliaires (bilirubine). Ils peuvent être exogènes (ce qui nous interesse) ; il s’agit alor de xénobiotiques divers fonctionnalisés (par des groupement fonctionnels tels que -OH, NH2, -COOH, -SH)
Réaction de substitution utilisant l’UDP-glucuronate comme réactif et une molécule peu polaire ayant un hydrogène mobile.
L’énergie nécessaire à la formation de la liaison osidique avec le substrat est fournie par la rupture de la liaison hémiacétal phosphorique de l’UDP-glucuronate. Il s’agit d’une réaction irréversible, catalysée par des enzyme.
III. Les enzymes de la glucuronoconjugaison : les glucuronyl-transférases.
1. Généralités:
Les UDP-Glucuronyl-transférases sont des enzymes réticulaires (situation : membrane du RE), et cytosoliques. Elles se retrouvent dans un grand nombre de tissus : foie, rein, intestin, peau, muqueuse nasale …
Elles possèdent une spécificité de substrat extrêmement large puisque des milliers de molécules différentes peuvent être qlucuronoconjuguées.
Il existe différentes isoenzymes des UDPGT (au moins 50), qui sont différenciées grâce à l’analyse des séquences en acides aminés.
Chez l’homme les glucuronyl-transférases sont classées en 2 grandes familles : les UDPG1 et UDPG2. Animaux ?
- Réactions catalysées, mécanisme d’action :
Ces enzymes catalysent les réaction de glucuronoconjugaison : formation d’une liaison osidique entre l’acide glucuronique et une molécule apolaire. Cette réaction permet l’élimination sous forme de glucuronides hydrosolubles de composés exogènes et endogènes. Les UGT de la famille 1A (UGT1A) sont majoritairement impliquées dans l’élimination des estrogènes et des catéchol-estrogènes. Les UGT sont exprimés dans le foie et au niveau du tractus gastro-intestinal, mais également dans les tissus cibles des stéroïdes tels la glande mammaire et la prostate.
UDP-Glucuronate + ROH à UDP + R-O-Glucuronate
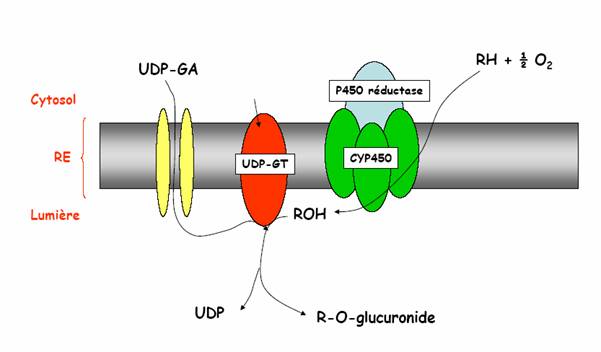
L’énergie nécessaire à la formation de la liaison osidique est fournie par la rupture de la liaison hémiacétal phosphorique de l’UDP-Glucuronate.
La réaction est IRREVERSIBLE !!!!!
Exemple : glucuronoconjugaison du phénol :
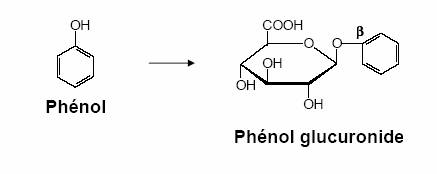
3. Variation, inductions
a) Variations :
o L’activité de certaines isoenzymes de l’UDPGT est très faible à la naissance puis augmente progressivement avec l’âge, probablement sous l’influence d’inducteurs hormonaux.
o D'origine pathologique : une atteinte hépatique sévère peut ralentir l'élimination de certains médicaments en raison d'une diminution de l'activité de certains enzymes qui les métabolisent. Par ailleurs, des troubles de la circulation hépatique ainsi qu'une diminution de la synthèse hépatique des protéines plasmatiques de transport s'ajoutent à la réduction de l'activité enzymatique pour ralentir l'élimination.
o Inter espèces : certaines espèces sont déficientes en certaines isoenzymes des UDPGT, et dans une espèce donnée, certaines souches peuvent être atteintes de ce déficit.
b) Induction :
Les UDPGT sont des enzymes inductibles : leur synthèse est accrue par des agents dits inducteurs, notamment de certains médicaments.
Cette induction a un certain nombre de conséquences, notamment :
- Elle rend compte de modifications du métabolisme de composés endogènes chez les sujets traités par des substances inductrices.
- Elle explique pourquoi la dose de certains médicaments doivent être augmentés progressivement : l’induction de UDPGT augmente la clairance de ces médicaments et leur concentration diminue plus rapidement dans l’organisme, donc leur efficacité est restreinte.
- De façon similaire aux cytochromes P450, l’expression et l’activité de glucuronoconjugaison catalysée par les isoenzymes UDPGTseraient modulées par des substances auxquelles l’organisme est couramment exposé : oestrogènes, hydrocarbures aromatiques polycycliques, flavonoides.
IV. Applications médicales
1. Variations de l’efficacité des glucuronoconjugaisons en fonction de l’espèce
Les glucuronoconjugaisons n’ont pas la même efficacité selon les espèces à cause de leur équipement enzymatique.
1.1- Ex pour les phénols (ne concerne pas les alcools, amines …) :
|
Espèce |
Glucuronoconjugaison |
|
Chat |
Très lente |
|
Chien |
Lente |
a. chez le chat
Le chat, déficient en glucuronyl-transférase des phénols, est sensible à tous les phénols :
- les salicylés et en particulier l'aspirine ;
- les phénicolés, éliminés après hydroxylation du cycle et glucuronoconjugaison
- le paracétamol : la toxicité de ce composé est particulière dans cette espèce (dès 50 mg/kg/j). On observe alors une anémie hémolytique.
La toxicité des phénols s’exprime en général par des troubles nerveux (convulsion, coma…) et des oedèmes pulmonaires.
Le chat n'est en revanche pas déficitaire en glucoronyl-transférases des alcools, acides, amines. De même, il possède les UDP-GT permettant la synthèse de glucuronides de stéroïdes, de bilirubine ou de thyroxine.
b. chez le chien
Les glucuronoconjugaisons chez le chien sont plus lentes, sans que cela entraîne pour autant des effets aussi importants que chez le chat.
![]()
![]()

1.2- Ex : l le rat Gunn
C’est une souche de rats albinos Wistar apparue en 1938. Ils présentent un déficit congénital en activité de glucuronoconjugaison hépatique, rénale ou intestinale de la bilirubine, alors que d’autres UDP-GT ont des activités « normales » ou faiblement diminuées. Il en résulte une accumulation de bilirubine dans l’organisme dont le signe le plus visible est un pelage jaunâtre. Cependant, la neurotoxicité de la bilirubine est beaucoup plus grave que les signes cutanés tout comme la néphropathie résultant de l’accumulation de la bilirubine dans la médullaire rénale. Ce sont les modèles d’une affection génétique de l’homme, la maladie de Crigler-Najjar de type 1.
2. Variations de l’efficacité des glucuronoconjugaisons en fonction de l’individu
a. Génétique
Tous les individus n'ont pas le même équipement enzymatique et la vitesse de métabolisation des médicaments peut s'en ressentir.
Les conséquences potentielles des variations génétiques au niveau du métabolisme des médicaments peuvent être :
- un effet pharmacologique prolongé,
- des effets indésirables,
- un manque d’activation de la pro-drogue,
- une toxicité,
- une augmentation de la dose efficace
- ou encore des interactions médicamenteuses exacerbées.
En effet, la variabilité génétique du taux d’expression ou de la fonction de ces enzymes a un impact très important sur l’efficacité du médicament. L’activation ou l’inhibition du métabolisme d’un médicament peut influencer sa concentration dans l’organisme, ainsi que celles de ses métabolites actifs, inactifs ou toxiques.
b. état physiologique
o L’âge
L'activité des enzymes peut varier au cours du développement. Chez le nouveau-né, la métabolisation des médicaments peut être plus lente que chez l'adulte.
Bien que ce ne soit pas la cause unique de l’ictère néonatal, la faible activité de l’UDP-GT vis-à-vis de la bilirubine est responsable d’un déficit de conjugaison de ce catabolite de l’hémoglobine et participe à sa faible élimination, et donc à l’apparition d’un ictère néonatal discret. Par exemple, chez le singe rhésus, à la naissance, l’activité de l’enzyme vis-à-vis des phénols est pratiquement identique à celle des adultes alors que vis-à-vis de la bilirubine elle est environ 20 fois plus faible.
o Le sexe
Elle peut également varier en fonction du sexe.
c. état pathologique
o Les affections hépatiques
Les affections hépatiques telles que les hépatites, les cirrhoses, les nécroses chimiques, les hépatocarcinomes… entraînent une diminution de l’activité de certaines glucuronyltransférases, d’où un ralentissement de l’élimination de certains médicaments.
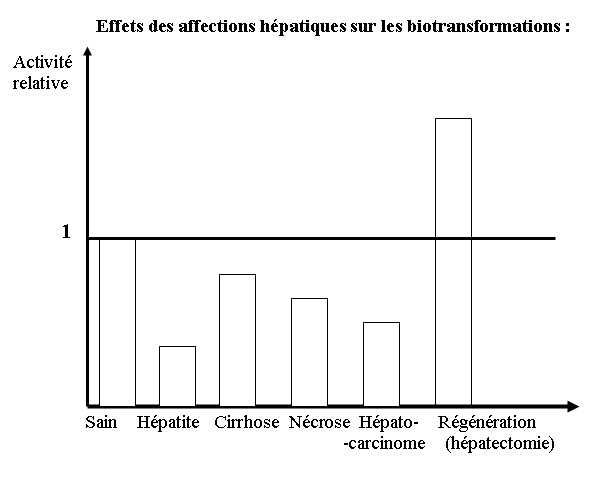
On peut remarquer que, lors de la régénération du foie (suite à une hépatectomie), l’activité des enzymes de biotransformations est augmentée.
o La maladie de Gilbert
La maladie de Gilbert de l’homme est une hyperbilirubinémie frappant près de 5% de la population. Les sujets atteints présentent également un métabolisme ralenti d’un certain nombre de médicaments. On observe que la proportion de diglucuronides de bilirubine diminue aux dépens des mono-glucuronides, traduisant une diminution de l’activité UDP-GT hépatique.
o Les carences
Enfin, on peut signaler que certaines carences, en protéines notamment, contribuent à la diminution de la synthèse des glucuronyl-transférases et par conséquent, à la diminution des glucuronoconjugaisons.
3. Variations de l’efficacité des glucuronoconjugaisons en fonction d’autres traitements
L'activité des enzymes peut être modifiée par la prise de certains médicaments. On observe soit une inhibition soit une induction.
a. Inhibition enzymatique
L'inhibition peut être recherchée ou fortuite et, dans ce cas, elle est souvent indésirable.
Lorsqu'elle est recherchée, on l'obtient par la prise d'un inhibiteur enzymatique.
Lorsqu'elle est fortuite, elle survient lors de la prise de médicaments non utilisés comme inhibiteurs enzymatiques mais qui peuvent cependant avoir une action inhibitrice. C’est par exemple le cas du furosémide (diurétique).
Furosémide
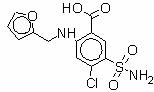
L'inhibition du catabolisme d'un médicament par un autre peut, dans des conditions particulières, être utilisée en thérapeutique, par exemple pour réduire la posologie d'un médicament coûteux. Il y a des exemples ?
b. Induction enzymatique
Les UDP-GT sont des enzymes inductibles ; leur biosynthèse est accrue sous l’effet d’agents dits inducteurs, notamment de certains médicaments tels que le phénobarbital, l’hexobarbital (des barbituriques) ou l’AZT (zidovuline ou 3’-azidothymidine).
Hexobarbital Phénobarbital
![]()
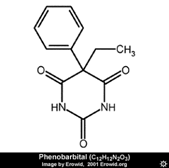
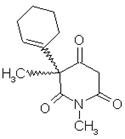
L'induction enzymatique a été mise en évidence initialement chez l'animal. On a constaté que des souris ou des rats qui avaient reçu quelques jours auparavant du phénobarbital devenaient insensibles à son effet hypnotique lors d'une administration ultérieure. On a montré que cette perte d'activité provenait essentiellement d'une métabolisation plus rapide du phénobarbital.
Cette induction a un certain nombre de conséquences vues précédement. Par exemple la dose de certains médicaments doit être progressivement augmentée : c’est par exemple le cas de l’AZT, utilisée dans le traitement des infections à FIV chez le chat.
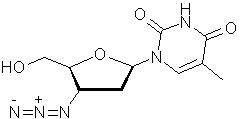
AZT
4. Autre application médicale
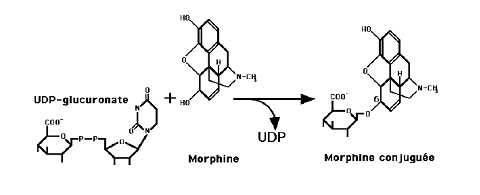
a. Cas de la morphine : Bioactivation du principe actif
Au niveau du foie, la morphine est transformée par glucuronoconjugaison en morphine-3-glucuronide inactif et dans une moindre mesure en morphine-6-glucuronide actif ; l’action de ce dernier composé est donc plus puissant, de plus il a la caractéristique de passer la barrière hémato-encéphalique. Ensuite, elle est excrétée en grande partie via l’urine sous forme de ces métabolites et le reste est excrété dans les fécès via la bile. La demi vie de la morphine peut être plus longue chez les sujets âgés. Etant donné son mécanisme d’excrétion, il convient de réduire les doses chez les patients atteint de maladies hépatiques ou d’insuffisance rénale.
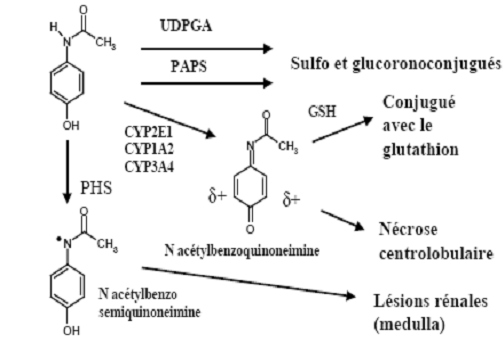
b. Cas du paracétamol (= acétominophène) : phénomène de saturation
Le paracétamol est largement
métabolisé par le foie en dérivés glucuronoconjugués (ou sulfoconjugués). Mais à
forte dose, ce composé peut s’avérer toxique. En effet, il s’agit d’un
phénomène de saturation : si on augmente progressivement la dose de
paracétamol, on aura d’abord une saturation des glucuronoconjugaisons et des
sulfoconjugaisons. Une faible fraction est alors
transformée par les cytochromes p450 en un métabolite très réactif, le
N-acétyl-p-benzoquinonéimine, qui réagit rapidement avec le glutathion
dont il diminue les concentrations. En cas de surdosage massif, cette réaction
devient importante et induit une déplétion en glutathion à l'origine d'un stress
oxydatif pouvant entraîner une nécrose centrolobulaire hépatique. La toxicité
hépatique impliquerait également une production de peroxynitrites à l'origine
d'un stress nitrosant.
![]()
Chez le chat, ce phénomène de saturation n’a pas le temps d’arriver car il y a oxydation des globules rouges ce qui entraîne leur lyse et une methémoglobination. On observe des muqueuses de couleur chocolat, une hémolyse urinaire et on assiste rapidement à la mort de l’animal.
Pour le chien, on se place dans une situation intermédiaire.
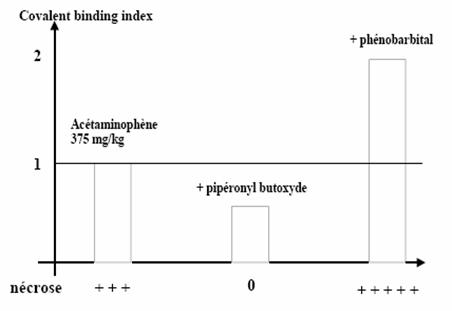
La toxicité du paracétamol est majorée chez les sujets présentant une induction enzymatique (barbituriques, alcool) ou une déplétion chronique en glutathion (dénutrition, alcoolisme chronique chez l’homme).
Par exemple, l’association du paracétamol avec le phénobarbital augmente la nécrose hépatique. L’association avec le pipéronyl butoxide (un inhibiteur des P450) entraîne une diminution de la formation de métabolites néfastes et a donc un effet protecteur.
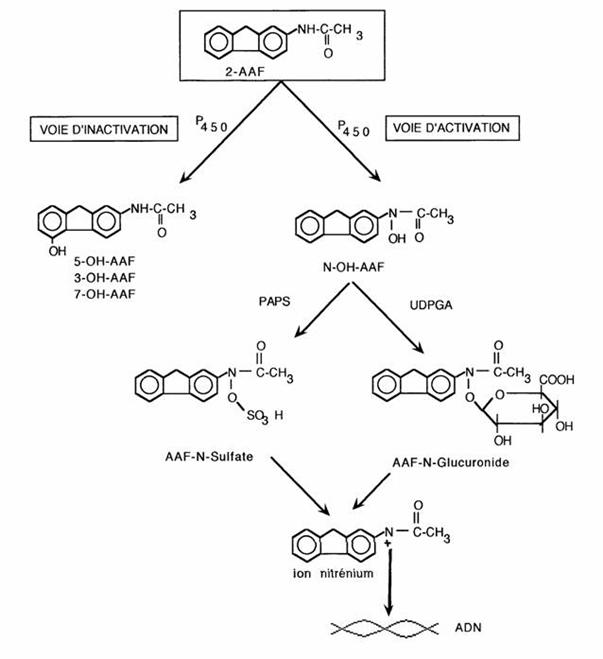
b. cas du 2-AAF : formation d’un composé toxique
La glucuronoconjugaison (ainsi que la sulfoconjugaison) des amines s'effectue après leur hydroxylation en hydroxylamines. Elle fournit des composés instables qui sont souvent l'objet de réarrangements intramoléculaires conduisant à la formation de métabolites toxiques.
C’est en particulier le cas du 2-AAF. Le AAF- N-Glucuronide formé par glucuronoconjugaison donne un ion nitrénium qui peut former un adduit avec l’ADN, d’où des conséquences toxiques de cette molécule.
Conclusions
Enzymes très importantes dans le métabolisme des médicaments et composés endogènes, toute induction ou inhibition peut avoir des répercussions.
En général métabolites formés conduisent à une excrétion urinaire et/ou biliare des composés
Dans de rares cas peut conduire à une bioactivation